Was sind Inhibitoren?
Inhibitoren sind Moleküle, die bei einer enzymkatalysierten Reaktion mit dem Substrat oder Ligand, um die Bindungsstelle am Enzym konkurrieren. Man unterscheidet grundsätzlich zwischen irrereversibler und reversibler Hemmung. Im ersten Fall bindet der Inhibitor unwiderruflich am Enzym, was einen Funktionsverlust des Enzyms zur Folge hat. Im zweiten Fall gibt es mehrere Mechanismen auf die im Folgenden noch detaillierter eingegangen wird. Trotz all der negativen Eigenschaften, die Inhibitoren zugesprochen werden, sind sie für den Organismus essentiell, da sie für viele regulatorische Prozesse im zellulären Stoffwechsel verantwortlich sind.
Wie funktionieren Inhibitoren?

Abbildung 1 Schematischer Mechanismus einer enzymkatalysierten Reaktion ohne Inhibitor. E=Enzym, ES=Enzym-Substrat-komplex, P=Produkt, k=Geschwindigkeitskonstante.
Irreversible Hemmung
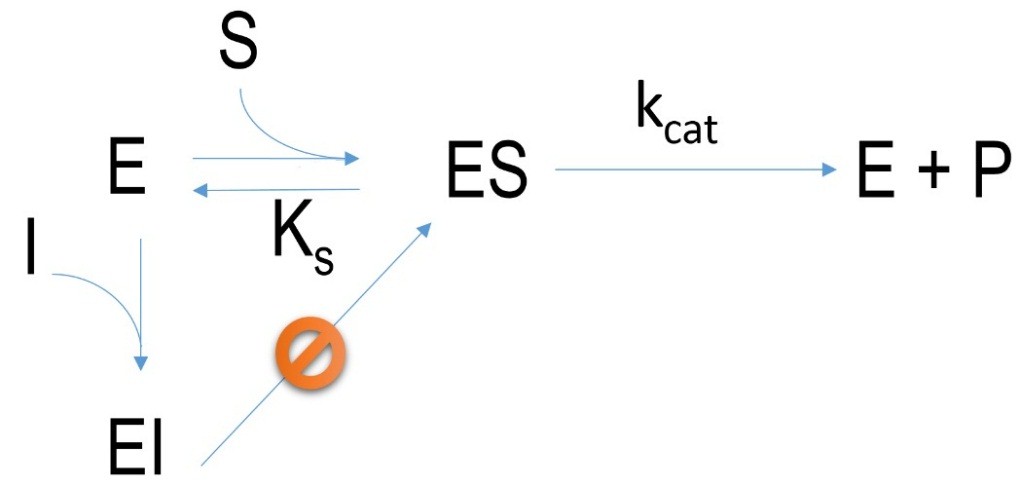
Abbildung 2 Schematischer Mechanismus einer irreversiblen Hemmung. E=Enzym, I= Inhibitor, EI=Enzym-Inhibitor-komplex, ES=Enzym-Substrat-komplex, P=Produkt, k=Geschwindigkeitskonstante, K= Dissoziationskonstante
Bei einer irreversiblen Inhibition bindet der Inhibitor kovalent an das aktive Zentrum. Diese Art der Inhibition kann nicht mehr aufgehoben werden. Viele irreversibel bindende Inhibitoren sind sogenannte „Suizid Inhibitoren“, da sie drastische physiologische Konsequenzen für den Organismus bedeuten. Beispiele für irreversibel bindende Inhibitoren (Saringas, Pestizide: DDT, Parathion, Antibiotika: Penicillin)
Reversible Hemmung
Kompetitiv
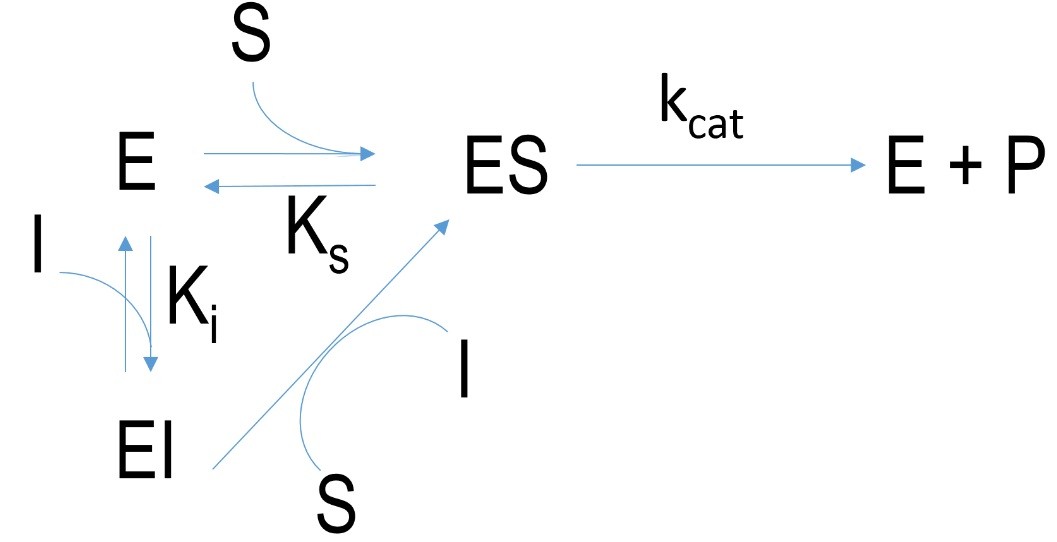
Abbildung 3 Schematischer Mechanismus einer kompetitiven Hemmung. E=Enzym, I= Inhibitor, EI=Enzym-Inhibitor-komplex, ES=Enzym-Substrat-komplex, P=Produkt, k=Geschwindigkeitskonstante, K=Dissoziationskonstante
Bei einer kompetitiven Inhibition bindet der Inhibitor auch an das aktive Zentrum, jedoch nicht kovalent, sodass eine schwächere Interaktion (H-Brückenbindungen, Ionenbindungen) stattfindet. Die Produktivität des Enzyms ist eingeschränkt. Dennoch kann durch Erhöhung der Substratkonzentration, im Kontrast zur irreversiblen Inhibition, diese Art der Hemmung überwunden werden.
Allosterisch oder nicht-kompetitiv
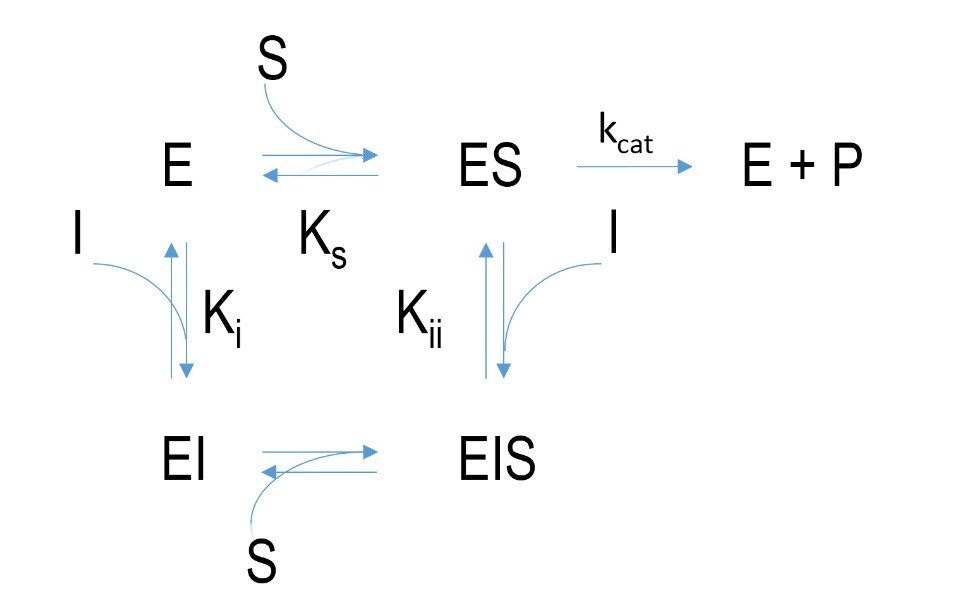
Abbildung 4 Schematischer Mechanismus einer nicht-kompetitiven Hemmung. E=Enzym, I= Inhibitor, EI=Enzym-Inhibitor-komplex, ES=Enzym-Substrat-komplex, EIS=Enzym-Inhibitor-Substrat-komplex P=Produkt, k=Geschwindigkeitskonstante, K= Dissoziationskonstante
Bei der allosterischen/nicht-kompetitiven Inhibition bindet der Inhibitor nicht direkt am aktiven Zentrum, sondern an einer anderen Stelle des Enzyms. Ein Enzym-Inhibitor-Komplex bildet sich. Dies hat eine Konformationsänderung des Enzyms zur Folge, was wiederum die Produktivität des Enzyms beeinträchtigt. Die Bindung des Inhibitors verhindert jedoch nicht die Bindung des Substrats, was ein wesentlicher Unterschied zur irreversiblen oder kompetitiven Inhibition ist. Neben der Bindung des Inhibitors am Enzym ohne Substrat, gibt es auch die Bildung eines Enzym-Substrat-Inhibitor-komplexes, d.h. der Inhibitor kann auch nach Substratbindung am Enzym binden. Dies kann zur Folge haben, dass das Produkt länger im aktiven Zentrum festgehalten wird. Bei der allosterischen Hemmung bietet die Erhöhung der Substratkonzentration keine Abhilfe.
Feedback Hemmung
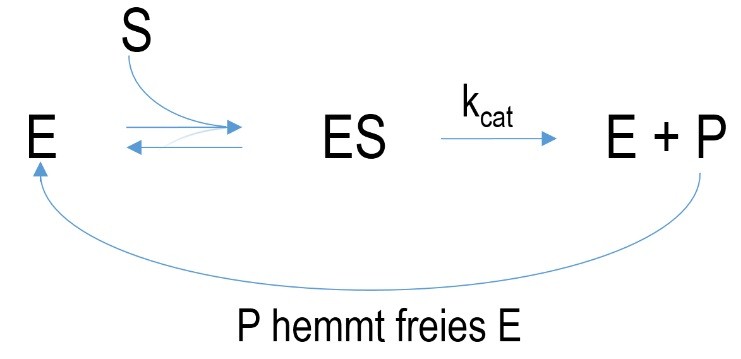
Abbildung 5 Schematischer Mechanismus einer Feedbackhemmung. E=Enzym, ES=Enzym-Substrat-komplex, P=Produkt, k=Geschwindigkeitskonstante, K= Dissoziationskonstante
Bei der Feedback Hemmung stellt das entstandene Produkt einer enzymkatalysierten Reaktion gleichzeitig den Inhibitor dar. Aufgrund dessen ist eine feine Regulierung der Substratumsetzung möglich, sodass eine Überproduktion verhindert wird.
Anwendung
Inhibitoren, im speziellen irreversibel-bindende, sind von großem Nutzen in der Pharmaindustrie, da sie einige Stoffwechsel-Enzyme sehr spezifisch hemmen können. Ein weiterer Vorteil besteht in der „Unreaktivität“ dieser Inhibitoren, außerhalb des aktiven Zentrums des Enzyms. Einige Vertreter sind z.B.:
DFMO (Difluor-methyl-ornithin): hemmt die Ornithin Decarboxylase der Trypanosomen, welche die Schlafkrankheit verursachen.
DFP (Diisopropyl-fluoro-phosphat): hemmt die Acetylcholinesterase, die im synaptischen Spalt Acetylcholin und Wasser in Cholin und Acetat spaltet.
Penicillin: hemmt die Glycopeptidtranspeptidase von Bakterien, welche für die Synthese der Zellwand verantwortlich ist. (1)
Weitere Gebiete, wo die Anwendung von Inhibitoren von essentieller Bedeutung ist, sind die Krebsforschung, die Erforschung bakterieller/viraler Infektionskrankheiten, sowie die generelle Erforschung von Mechanismen bei enzymkatalysierten Reaktionen.
Literatur
- http://www.chemgapedia.de/vsengine/vlu/vsc/de/ch/8/bc/vlu/biokatalyse_enzyme/enzymhemmung.vlu/Page/vsc/de/ch/8/bc/enzymregulation/suicide_inh.vscml.html Stand: 04.04.2016 15:30
- Stryer et al. Biochemisty 5th edition, K.8.5, S. 330-335
- Campbell and Reece, Biology 8th Edition, K. 8.4, S. 156



